أعادت دراسة حديثة، منشورة بتاريخ 11 سبتمبر/أيلول في دورية نيتشر بايوتكنولوجي، كتابة الأبجدية الجينية بهدف تخليق بروتينات جديدة غير موجودة في الطبيعة باستخدام تقنيات مبتكرة. الدراسة أجراها علماء معهد سكريبس الأميركي للأبحاث، يقودهم الباحث المصري أحمد بدران، الأستاذ المساعد في قسم البيولوجيا البنيوية والحسابية التكاملية في المعهد.
يقول ماثيو هارتمان، أستاذ الكيمياء العضوية في قسم الكيمياء في جامعة فيرجينيا كومنولث، بالولايات المتحدة الأميركية، في تصريح حصلت الجزيرة نت على نسخة منه: “إن جمال المفهوم المقدم في هذه الدراسة هو أنه من السهل دمجه في العديد من أنواع العمليات لأنه يتطلب فقط تصميما مدروسا للجينات”.
الشفرة الجينية الثلاثية
تعمل الخلية الحية عبر آلية تتلخص في إنتاجها لبروتينات محددة والتي من خلالها تؤدي وظائفها وتتفاعل مع محيطها. الإنسولين على سبيل المثال، هو بروتين تفرزه خلايا البنكرياس في الدم للحفاظ على مستويات السكر فيه. يتكون ذلك البروتين داخل خلايا بيتا بالبنكرياس عبر آلية عامة، تستخدمها غالبية خلايا الجسم وخلايا بقية الكائنات الحية لأداء وظائفها المختلفة.
البروتين هو كل شيء في أجسادنا، بداية من مكونات عضلاتنا ووصولا إلى أدق التكوينات العاملة في الخلايا الصغيرة، ولبنائه تترجم الخلية جزءا محددا من الشفرة الوراثية (دنا) الموجودة داخل نواتها إلى أحماض أمينية، والتي تمثل الوحدات الأولية التي تكوّن البروتين، وترتبط تلك الأحماض معا لتكوّن أيا من البروتينات المعروفة.
لفهم الأمر تخيل أن أحد الأفلام المشوقة موجود الآن على حاسوب صديقك، ستستأذنه في الحصول عليه عبر أداة تخزين بحجم عقبة الأصبع (فلاش ميموري) ثم تشغله على حاسوبك، الفيلم مكتوب على أداة التخزين بلغة خاصة، يترجمها حاسوبك فيظهر الفيلم على الشاشة.
هذا بدرجة من التبسيط هو ما يحدث لتخليق البروتينات في أجسامنا، حيث يتم تخليق الأحماض الأمينية عبر شفرة ثلاثية، أي تتكون من 3 حروف فقط، تُعرف باسم الكودون. وكل كودون هو رمز مخصص لحمض أميني معين، فمثلا حمض التريبتوفان الأميني مكانه يترجم باستخدام كودون ثلاثي مكون من الحروف الثلاثة “يو جي جي” (UGG)، كما يمكن استدعاء الميثايونين باستخدام “إيه يو جي” (AUG)، وبذلك يؤدي كل تعاقب وتغيير في ترتيب الحروف الكيميائية الأربعة الأساسية وهي “إيه” (A) و”يو” (U) و”جي” (G) و”سي” (C) في الكودون إلى بناء حمض أميني مختلف.
إعادة كتابة الأبجدية الجينية
نجح بدران وفريقه في إعادة كتابة الأبجدية الجينية الثلاثية المخصصة لاستدعاء الأحماض الأمينية الأساسية الـ20، وجعلها رباعية، والهدف ببساطة هو استدعاء أحماض أمينية غير أساسية إضافية، وهذا سيزيد من التنوع الحيوي عبر خلق بروتينات لم تكن موجودة في الطبيعة من قبل.
يقول بدران، في تصريحات خاصة للجزيرة نت: “اكتشفنا مبادئ يمكن هندستها وتطبيقها بسهولة على “رنا المرسال” لتحسين كيفية قراءة الريبوسوم لتسلسلات القواعد الرباعية. ومن خلال دمج العديد من الأحماض الأمينية غير التقليدية المختلفة في نفس البروتين، سنكون قادرين على إنتاج بروتينات تتمتع بكيمياء تتجاوز تلك المتاحة في الطبيعة”.
أجرى الفريق عملية تعرف باسم “ضغط الكودون”، وهي وضع الكودونات الثلاثية “عالية الاستخدام” حول الكودونات الرباعية، بشكل يساهم في تحسين كفاءة فك التشفير بشكل كبير. وهو ما ساعد على قراءة الريبوسوم (جسيم دون خلوي يساهم في تلك العملية) للكودونات الرباعية بشكل صحيح، وهذا سمح بدمج الأحماض الأمينية غير التقليدية المرغوبة بنجاح.
ويشير مصطلح الكودون “عالي الاستخدام” إلى الكودون الذي تستخدمه الخلية الحية بشكل متكرر لتشفير أحماض أمينية معينة أثناء تخليق البروتين. هذه الكودونات مفضلة لأنها تعزز كفاءة عملية الترجمة إلى أحماض أمينية، وهذا يعني أن الريبوسوم قادر على قراءتها بسهولة وسرعة أكبر، وهذا يؤدي إلى عملية إنتاج بروتين أكثر فعالية.
ولاحظ الباحثون تفضيلا خلويا للكودونات عالية الاستخدام عندما تأتي مباشرة بعد الكودونات الرباعية. وألهمتهم هذه الملاحظة لمتابعة نهج إعادة التشفير الجيني الاصطناعي، حيث استخدموا كودونا واحدا عالي الاستخدام لكل حمض أميني في عناصر تشفير البروتين في الجدول الجيني، وبذلك أصبح هناك كودون ثلاثي واحد لكل من الأحماض الأمينية القياسية الـ20 وكودون رباعي لكل حمض أميني غير تقليدي. وبمزيد من الجهد، تمكن الفريق من دمج 47 حمضا أمينيا غير أساسي فريدا في بروتينات.
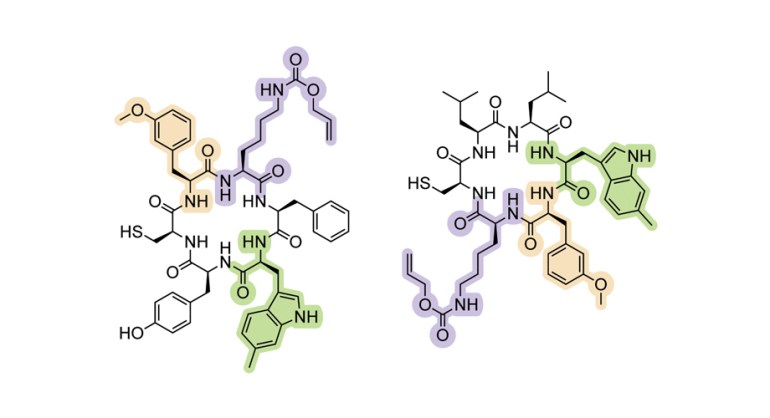
عالم جديد من البروتينات المستحدثة
يقول بدران: “كنت متحمسا لإمكانات البروتينات والببتيدات الجديدة على الطبيعة لبعض الوقت، وأعتقد أن تحسين كيفية الوصول إلى مثل هذه الجزيئات المتنوعة كيميائيا سيسمح للباحثين بتطوير جيل جديد من العلاجات. وتتوافق هذه الدراسة -التي آمل أن تكون الأولى من بين العديد- بقوة مع هذا الاعتقاد”.
لإثبات فائدة هذا النهج في الخلايا، ركز الفريق عمله على التخليق الحيوي لما يسمى “الببتيدات الحلقية الكبيرة القابلة للبرمجة” لثباتها العالي؛ وهي خاصية مهمة للمركبات الكيميائية، وقد نجح باحثو معهد سكريبس في دمج 3 أحماض أمينية غير تقليدية مميزة في بروتينات حلقية كبرى مصنعة بيولوجيا، وهذا غيّر من خصائصها الكيميائية بنجاح.
يقول بدران: “تكمن القوة الحقيقية لتقنيتنا في بساطتها مقارنة بالنماذج السابقة، ولسنا أول مجموعة تستكشف فك التشفير الرباعي، فقد كان البروفيسور تشين وبيتر شولتز هنا في معهد سكريبس للأبحاث رائدين في هذا المجال، ونحن نبني على عملهما السابق. ورؤيتنا طويلة المدى هي التوسع في هذا النهج لإنشاء بروتينات حلقية كبيرة متنوعة كيميائيا وذات أنشطة مستحدثة”.
نشأ بدران في مدينة طنطا المصرية ثم هاجر إلى الولايات المتحدة خلال سنوات دراسته الثانوية. ومنذ ذلك الحين، درس الكيمياء الحيوية وعلم الأحياء الجزيئي في جامعة أريزونا، بالإضافة إلى علم الكيمياء الحيوية والتطور الموجه في جامعة هارفارد، وعلم الأحياء الاصطناعي التطبيقي في معهد ماساتشوستس للتكنولوجيا/معهد برود.
يقول بدران: “خلال هذه الفترة، عشت في العديد من أنحاء العالم ورأيت كيف يمكن للتقدم العلمي أن يفيد البشرية جمعاء، وقد شكل هذا المثل الأعلى نهجي في العلوم. على سبيل المثال، كانت نشأتي في مصر والعيش في أريزونا في الولايات المتحدة الأميركية بمثابة القوة الدافعة لعمل مختبري على تحسين تغير المناخ باستخدام هندسة البروتين، حيث تتعرض هذه الأجزاء من العالم لأعظم تهديد من ارتفاع درجات الحرارة العالمية”.